Vivre avec votre CGM
Quelles sont les causes de l’hyperglycémie nocturne et avant le petit déjeuner?
Cet article vous permet de comprendre les causes d’une hyperglycémie nocturne et avant le petit déjeuner et vous apprend comment y faire face.
Vivre avec votre CGM
Cet article vous permet de comprendre les causes d’une hyperglycémie nocturne et avant le petit déjeuner et vous apprend comment y faire face.

Dans certaines situations, les raisons d’une hyperglycémie matinale ou d’une hausse importante de la glycémie durant la nuit sont évidentes. Cependant, on observe occasionnellement des cas où les causes de ces fluctuations demeurent peu claires. Cet article vise à vous présenter les raisons possibles de votre hyperglycémie afin de vous en donner une meilleure compréhension et vous fournir des astuces pour mieux l’éviter.
Le mieux est de commencer à analyser vos valeurs CGM nocturnes en début de nuit, c-à-d avant d’aller au lit. Vos valeurs avant le coucher se situent-elles encore dans votre intervalle de référence ou entamez-vous la nuit avec des valeurs déjà élevées? Être dans votre objectif glycémique, c-à-d avoir des niveaux de glucose en dessous de 10 mmol/L avant de vous coucher est une première étape importante vers de bonnes valeurs pendant la nuit.1
Si vos valeurs de glucose sont toutes généralement trop élevées, même durant la journée, nous vous recommandons de vous consulter avec votre équipe médicale afin d’évaluer si votre traitement actuel est toujours adapté. Nous vous invitons également à lire l’article «Quelles sont les causes d’une hyperglycémie pendant la journée?».
Entamez-vous la nuit avec une valeur de glucose déjà élevée? Si cela est le cas, vous avez peut-être grignoté un en-cas en fin de soirée et vous avez oublié de vous injecter une quantité suffisante d’insuline, ou vous avez sous-estimé la teneur en glucides de votre souper. Ou alors vous avez utilisé un rapport glucides/insuline non adapté pour le repas du soir. Un souper bien copieux peut lui aussi être la cause de vos valeurs élevées, car son effet hyperglycémiant peut demeurer pendant quelques heures après le repas. Dans ce cas, il est utile de garder un intervalle de 3 à 4 heures entre le dernier repas copieux et l’heure du coucher.
💡 Pour obtenir une bonne valeur de glucose à jeun, il est essentiel que la valeur avant le coucher soit inférieure à 10 mmol/L.
Une cause très fréquente d’une augmentation des valeurs de glucose pendant la nuit est une quantité insuffisante d’insuline basale, qui ne permet pas de maintenir votre glycémie stable. L’utilisation d’un système de mesure en continu du glucose (CGM) vous permet de vérifier facilement ce phénomène, notamment si votre glycémie augmente quasiment chaque nuit en l’absence d’autres causes telles celles préalablement mentionnées (un souper ou du grignotage tard le soir).2
Habituellement, le foie et les reins sécrètent en permanence une certaine quantité de glucose dans le sang. Ce phénomène a lieu entre les repas et durant la nuit et sert à maintenir stables les niveaux de glycémie ainsi qu’à garantir les fonctions de base du corps.
En fonction du poids, environ 8 à 12 g de glucose par heure sont sécrétés dans le sang.6 Si vous présentez une résistance à l’insuline (ce qui est souvent le cas chez les personnes souffrant de diabète de type 2), cette quantité peut être considérablement plus élevée. Pour transporter ce glucose dans les cellules, il faut de l’insuline.
Un niveau basal d’insuline est nécessaire pour garantir un approvisionnement continu en glucose des cellules. Les besoins en insuline peuvent bien entendu varier au cours du temps, de manière temporaire ou permanente. Une modification passagère du niveau d’insuline basale s’observe par exemple lors d’une infection, en cas de fièvre, d’allergies ou suite à un traitement à base de cortisone.
Une augmentation des besoins en insuline basale peut toutefois également s’installer progressivement au fil des mois et des années, par exemple en cas de prise de poids, avec l’âge ou suite à des changements hormonaux tels que la ménopause.
💡Si vous avez l’impression que votre approvisionnement en insuline basale nocturne est insuffisant, faites-en part à votre équipe médicale afin d’évaluer un ajustement éventuel de votre traitement.
Une résistance à l’insuline est couramment observée chez les personnes souffrant de diabète de type 2 et/ou en surpoids (notamment en présence de graisse abdominale). «Résistance à l’insuline» signifie que les cellules et organes ne sont plus en mesure de répondre correctement à cette hormone (l’insuline).
En cas de résistance à l’insuline, le foie libère davantage de glucose dans le sang. Les cellules étant incapables de répondre à l’insuline, elles ne sont pas en mesure d’absorber le glucose, qui va donc s’accumuler dans le sang. Par conséquent, les valeurs de glucose seront élevées pendant la nuit et au matin, même en étant à jeun. Chez certaines personnes, le taux de glucose n’arrive pas à atteindre des valeurs comprises dans l’intervalle de référence (objectif glycémique) en dépit de doses élevées d’insuline, ce qui peut être très frustrant.
💡En cas d’hyperglycémie due à une résistance à l’insuline, le problème ne pourra pas être résolu uniquement par un traitement insulinique, car les cellules ne sont pas en mesure d’utiliser l’insuline de manière efficace.
Les astuces suivantes peuvent vous aider à améliorer la résistance à l’insuline:
Essayez d’intégrer autant que possible une activité physique à votre quotidien: une promenade de 20 minutes après le souper peut impacter favorablement votre glycémie à jeun, et ce de manière considérable. L’exercice physique améliore la sensibilité des cellules à l’insuline: cela leur permet d’assimiler le glucose plus facilement, réduisant ainsi le besoin en insuline. Pour en savoir plus à ce sujet, nous vous invitons à consulter l’article «Quels sont les effets de l’activité physique sur le corps et les valeurs de glucose?».
L’un des facteurs principaux responsables de la résistance à l’insuline est la graisse abdominale. À chaque kilo perdu, vos cellules et votre foie redeviennent plus sensibles à l’insuline et votre glycémie à jeun s’améliore. Votre équipe soignante se fera un plaisir de vous aider pour toute question concernant des médicaments antidiabétiques favorisant la perte de poids. Pour en savoir plus sur une alimentation saine et équilibrée, nous vous invitons à consulter l’article «Quels aliments privilégier en cas de diabète mellitus?».
Les régimes à base de flocons d’avoine sont une alternative assez drastique permettant de rétablir la réponse de votre corps à l’insuline. Pendant 2 ou 3 jours, vous remplacez vos trois repas par 60 à 80 g de flocons d’avoine cuits dans un demi-litre d’eau ou de bouillon allégé en matières grasses. Pour varier le goût, vous pouvez y ajouter jusqu’à 50 g de fruits ou une quantité abondante de légumes; les aliments ou condiments gras sont tabou. L’objectif est de réduire drastiquement l’apport en calories pour brûler la graisse stockée dans le foie et le pancréas. Une fois cette graisse éliminée, le foie recommence souvent à répondre à l’insuline et ne sécrète plus de glucose dans le sang de manière incontrôlée.
Les effets bénéfiques des cures à base de flocons d’avoine peuvent se maintenir durant plusieurs semaines. Pour bénéficier de ces effets par la suite, vous pouvez répéter la cure3. Cela peut nécessiter un ajustement de votre traitement ou de votre dose d’insuline: dès lors, nous vous recommandons de consulter préalablement votre médecin traitant avant de tester cette méthode.
Les glucides ne sont pas les seuls nutriments susceptibles d’augmenter votre glycémie. Saviez-vous que les repas riches en graisses et protéines pouvaient également entraîner une hausse de votre glycémie avec effet différé? Si vous participez à une soirée barbecue en été et que vous mangez plus de viande qu’à votre habitude, ou si vous vous autorisez une bonne portion de noix devant la télé, vous risquez de voir vos valeurs de glucose grimper pendant la nuit.
En fonction de la quantité de graisses et de protéines que vous consommez, le glucose peut augmenter après 3 à 8 heures1. Certains constituants des protéines (les acides aminés) ayant un impact sur la glycémie sont eux-mêmes transformés en glucose. Par ailleurs, d’autres acides aminés entraînent une augmentation de la libération de glucagon, ce qui pousse le foie à libérer davantage de glucose.
💡 Si vous remarquez un lien entre des repas riches en lipides et protéines et une augmentation de vos valeurs CGM durant la nuit, n’hésitez pas à prendre contact avec votre équipe médicale afin de comprendre s’il faudrait prendre en compte celles que l’on appelle les «unités de gras/protéines». Si vous êtes sous traitement par pompe à insuline, un bolus duo ou mixte peut vous aider à compenser l’augmentation retardée de la glycémie due à l’apport en unités de gras/protéines. Si votre administration d’insuline se fait par injection, il pourrait être nécessaire, dans certaines circonstances, de répartir la dose d’insuline destinée à corriger l’apport en unités de gras/protéines sur deux injections distinctes.
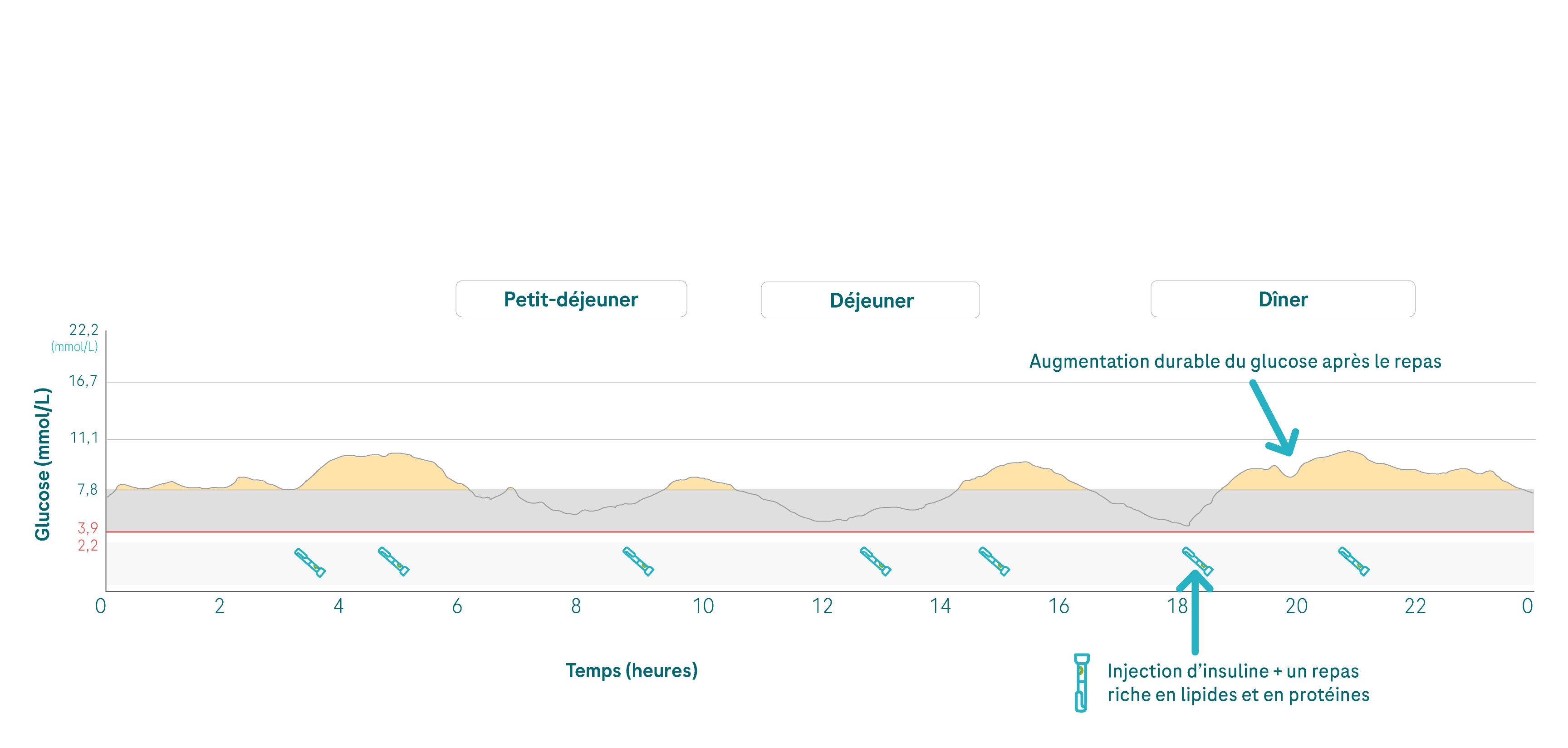
Un repas à base de lipides et protéines (par ex. un souper avec du poisson) peut entraîner une augmentation de la glycémie pendant jusqu’à 6 heures après le repas.
Il peut nous arriver de mal dormir ou de ne pas dormir suffisamment, car nous sommes tourmentés par nos problèmes et les ruminons toute la nuit. Saviez-vous qu’un sommeil insuffisant ou perturbé pouvait entraîner une glycémie à jeun élevée? La durée de sommeil recommandée est de 7 à 9 heures par nuit3. Si votre durée de sommeil est plus courte, ou si vous avez du mal à dormir, vos besoins en insuline et votre appétit peuvent augmenter.
Le phénomène de l’aube se produit lorsque les valeurs de glucose se situent, dans un premier temps, dans les objectifs glycémiques jusqu’aux premières heures du matin, mais augmentent ensuite brusquement entre 3h et 6h du matin. Sans un dispositif CGM, vous ne seriez en mesure de détecter cette variation qu’au moment d’une mesure de la glycémie pendant la nuit. En revanche, grâce au capteur CGM vous pouvez reconnaître le phénomène de l’aube beaucoup plus facilement.
La hausse des valeurs de glucose au petit matin est due à une augmentation de la sécrétion d’hormones de croissance, de cortisol et de glucagon. Ces hormones réduisent l’effet de l’insuline en raison de leur action antagoniste, c-à-d qui s’oppose à l’action de l’insuline. Une certaine augmentation du taux d’hormones tôt le matin est physiologique – toutefois, ce phénomène est accru chez certaines personnes.
💡 Souvent, un traitement à base d’insuline basale classique ne permet pas de contrer ce phénomène de façon efficace. Pour résoudre ce problème, vous devez passer à une autre insuline basale et vous administrer un analogue d’insuline à action rapide en petites doses en tout début de matinée (par ex. à 4h), à condition que vous vous réveilliez à cette même heure. Vous pouvez également utiliser une pompe à insuline dispensant l’insuline en fonction des besoins de votre corps. Nous vous invitons à vous consulter avec votre équipe médicale afin d’évaluer l’option la plus adaptée à vos besoins.
Lors du phénomène du «pied au sol» ou du «lever», la glycémie augmente immédiatement après le lever. Comme dans le cas du phénomène de l’aube, cette augmentation rapide est due aux hormones. Après le lever, l’organisme secrète progressivement plus d’hormones dans le but de stabiliser la tension artérielle après le passage de la position horizontale pendant le sommeil à la position verticale. Ces hormones diminuent la sensibilité à l’insuline.
💡Le capteur CGM vous permet de déceler ces hausses marquées directement après le lever. Consultez votre équipe médicale afin d’évaluer si une petite dose d’insuline à action rapide avant le lever pourrait vous aider à éviter ces augmentations de la glycémie.
L’hypoglycémie nocturne peut également être à l’origine d’une glycémie à jeun élevée. En cas d’hypoglycémie, de l’adrénaline est sécrétée, ce qui entraîne une libération de glucose par le foie et provoque une augmentation différée de la glycémie. En cas d’hypoglycémie, on a également tendance à boire trop de jus ou à consommer trop de glucose ou de sucreries.
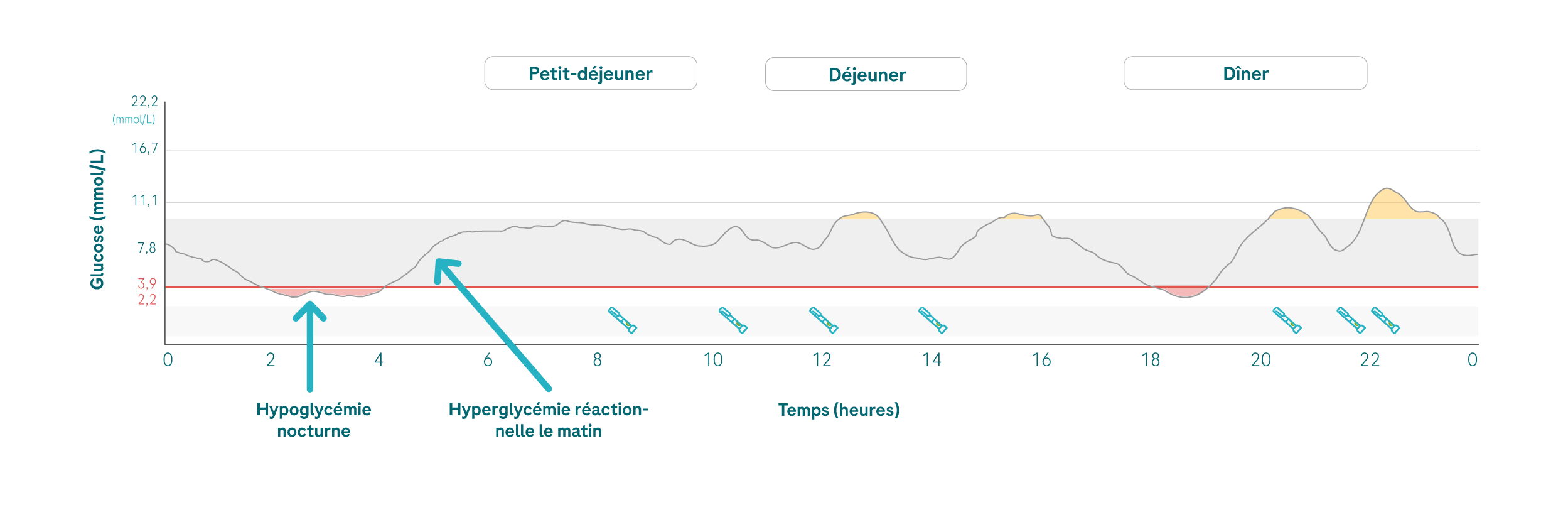
💡En premier lieu, il est essentiel de trouver la cause de l’hypoglycémie nocturne. N’ayez pas de réaction trop hâtive ou excessive et ne corrigez pas l’hyperglycémie avec une dose trop importante d’insuline. Le foie récupère le glucose initialement sécrété dans le sang par effet différé, ce qui peut entraîner une nouvelle hypoglycémie.
Beaucoup de personnes diabétiques préfèrent s’injecter l’insuline au même site d’injection et n’aiment pas trop changer leurs habitudes. Une sollicitation répétée des mêmes zones de la peau et, par ailleurs, une réutilisation de l’aiguille peuvent altérer le tissu. Cela s’applique également à l’utilisation d’une pompe à insuline, car souvent les patients insèrent le dispositif de perfusion au même site d’injection. De telles habitudes se traduisent souvent en un durcissement palpable du tissu et, dans certains cas, en un épaississement visible appelé lipohypertrophie. Si vous injectez de l’insuline dans une zone de la peu ayant développé une lipohypertrophie, la concentration d’insuline relevée dans le sang peut être réduite d’un tiers par rapport à la concentration en insuline observée après injection dans un tissu sain. Les valeurs de glucose mesurées après un repas seront alors beaucoup plus élevées.5
💡Palpez les sites d’injection pour vous assurer de l’absence de gonflements caoutchouteux et d’indurations non visibles à l'œil nu. Évitez ces sites d’injection jusqu’à ce que le tissu soit rétabli – cela peut prendre des mois, voire des années. Lorsque vous changez de site d’injection, une réduction de votre dose d’insuline peut être nécessaire. À ce propos, nous vous invitons à vous consulter avec votre équipe médicale.
Les meilleures stratégies pour éviter une aggravation de la lipohypertrophie sont les suivantes:
Pour obtenir un effet constant et homogène de l’insuline chaque nuit, il est important de bien mélanger les insulines troubles (laiteuses) avant de les injecter. Ce type d’insuline est destiné à l’injection dans la cuisse, le soir avant d’aller se coucher. En revanche, les analogues d’insuline à action prolongée ne doivent pas être mélangés et peuvent être injectés directement, dans l’abdomen ou la cuisse.
Garder un œil attentif sur vos valeurs de glucose et vos habitudes peut donc vous être très utile afin de repérer les causes des hyperglycémies nocturnes et matinales. À cet égard, un dispositif CGM peut s’avérer un véritable soutien, car il vous permet de comprendre ce qui se passe réellement pendant votre sommeil.

Injection dans une zone de lipohypertrophie au niveau de l’abdomen.
[1] American Diabetes Association Professional Practice Committee; 6. Glycemic Goals and Hypoglycemia: Standards of Care in Diabetes—2024. Diabetes Care 1 January 2024; 47 (Supplement_1): S111–S125. https://doi.org/10.2337/dc24-S006
[2] Thomas, Andreas et al. (2019). CGM interpretieren: Grundlagen, Technologie, Charakteristik und Konsequenzen des kontinuierlichen Glukosemonitorings (CGM) (2. Aufl.). Mainz
[3] Delgado G, Kleber ME, Krämer BK, Morcos M, Humpert PM, Wiegand K, Mauldin A, Kusterer K, Enghöfer M, März W, Segiet T, Lammert A. Dietary Intervention with Oatmeal in Patients with uncontrolled Type 2 Diabetes Mellitus - A Crossover Study. Exp Clin Endocrinol Diabetes. 2019 Oct;127(9):623-629. doi: 10.1055/a-0677-6068. Epub 2018 Aug 29. PMID: 30157531.
[4] Watson NF, Badr MS, Belenky G, Bliwise DL, Buxton OM, Buysse D, Dinges DF, Gangwisch J, Grandner MA, Kushida C, Malhotra RK, Martin JL, Patel SR, Quan SF, Tasali E. Recommended Amount of Sleep for a Healthy Adult: A Joint Consensus Statement of the American Academy of Sleep Medicine and Sleep Research Society. Sleep. 2015 Jun 1;38(6):843-4. doi: 10.5665/sleep.4716. PMID: 26039963; PMCID: PMC4434546.
[5] Famulla S, Hövelmann U, Fischer A, Coester HV, Hermanski L, Kaltheuner M, Kaltheuner L, Heinemann L, Heise T, Hirsch L. Insulin Injection Into Lipohypertrophic Tissue: Blunted and More Variable Insulin Absorption and Action and Impaired Postprandial Glucose Control. Diabetes Care. 2016 Sep;39(9):1486-92. doi: 10.2337/dc16-0610. Epub 2016 Jul 13. PMID: 27411698.
[6] Malcolm Watford (2023), Encyclopedia of Human Nutrition : Glycogen breakdown and gluconeogenesis provide glucose to the body (Fourth Edition)
Vous souhaitez être toujours à jour ? Inscrivez-vous gratuitement dès maintenant !