Vivre avec votre CGM
Quelles sont les causes de l’hyperglycémie pendant la journée?
Cet article vous permet de comprendre les causes d’une hyperglycémie diurne et vous apprend comment y faire face.
Vivre avec votre CGM
Cet article vous permet de comprendre les causes d’une hyperglycémie diurne et vous apprend comment y faire face.

Des niveaux de glucose élevés représentent une lourde charge et sont souvent difficiles à appréhender. Afin de bien comprendre les mécanismes du métabolisme, il est avant tout important de savoir qu’une augmentation des valeurs de glucose, telle que celle observée dans le sang, ne résulte pas exclusivement des glucides ingérés sous forme de nourriture ou de boissons. Si cela était le cas, la gestion de la glycémie serait un exercice de calcul mathématique, facile à compenser avec précision.
La situation se complique davantage si l’on considère que, en effet, l’organisme stocke généralement les glucides dans les muscles, les reins et le foie sous forme de glycogène, prêt à être libéré dans le sang au besoin. Souvent, il est impossible de prévoir si et quand le corps libérera ces réserves de glucose naturel (également appelé «glucose endogène»). C’est pourquoi il est si difficile de maintenir en permanence un niveau de glucose dans ses intervalles de référence (objectif glycémique).
Dans cet article, nous avons répertorié un aperçu des causes et explications les plus probables d’une hyperglycémie (des valeurs élevées de glucose) pouvant survenir au cours de la journée. Grâce à la quantité considérable de données récoltées et aux graphiques prévisionnels générés, le dispositif de mesure en continu du glucose (CGM) vous permet d’identifier ces causes plus facilement. La première étape consiste à distinguer entre les valeurs avant et après un repas.
Si vos valeurs de glucose sont régulièrement élevées même avant un repas, il se peut que votre couverture en insuline basale soit insuffisante, notamment si l’on peut exclure que le repas précédent soit à l’origine de ces valeurs élevées. L’insuline basale sert à compenser la libération continue de glucose par le foie et les reins, nécessaire à garantir l’approvisionnement en énergie de l’organisme entre les repas. Différents facteurs peuvent induire une variation des besoins en insuline au fil du temps: il est donc important de vérifier régulièrement vos besoins en insuline basale en cas de valeurs de glycémie élevées.
Vos besoins en insuline peuvent parfois varier temporairement suite à des événements tels que le stress, une infection, des allergies, le cycle menstruel ou un traitement à base de cortisone. Cependant, une augmentation des besoins en insuline basale peut également s’installer progressivement et de manière insidieuse, par exemple en cas de prise de poids, avec l’âge ou suite à des changements hormonaux tels que la ménopause.
💡Sans dispositif CGM, il vous faudrait sauter des repas et mesurer votre glycémie toutes les heures pour arriver à détecter une couverture insuffisante en insuline basale. En revanche, une solution CGM vous facilite la tâche de manière considérable. Si vous remarquez que vos valeurs sont élevées avant le repas ou que votre glycémie augmente même sans avoir ingéré de glucides, n’hésitez pas à consulter votre équipe médicale afin d’évaluer un ajustement éventuel de votre traitement.
Parfois, nous sommes parfaitement conscients du stress. À d’autres moments, au contraire, nous pouvons être stressés sans vraiment nous en rendre compte. En situation de stress ou lors d’une charge mentale importante, notre cerveau requiert jusqu’à 30% d’énergie supplémentaire et notre corps libère des hormones du stress telles que l’adrénaline, la noradrénaline et le cortisol, ainsi que du glucagon dans un deuxième temps. Ces hormones entraînent une augmentation du taux de glucose induite, d’un côté, par l’inhibition de l’action de l’insuline et, de l’autre côté, par une stimulation du foie et des reins à relâcher davantage de glucose dans le sang. Cette libération endogène (par le corps même) d’insuline se manifeste par des fluctuations très marquées de la glycémie visibles dans votre graphique de tendance CGM, avec des hausses pouvant atteindre les 3,3 mmol/L en l’espace de 20 minutes1. En cas de stress aigu, vous pouvez souvent observer dans vos graphiques CGM une augmentation parallèle de vos valeurs de glucose et du stress.
💡 Essayez de réduire ou d’éviter le plus possible les facteurs de stress. Réfléchissez à comment réduire ou éviter les facteurs favorisant le stress. Si vous êtes affecté par le stress sur une période prolongée, demandez conseil à votre équipe médicale afin d’évaluer un éventuel ajustement de votre dose d’insuline pour compenser le besoin accru. Gardez toutefois à l’esprit que des valeurs temporairement élevées de glycémie ne sont dues qu’au glucose mis à disposition par le foie, qui va le récupérer ultérieurement afin de reconstituer ses réserves. À ce moment-là, le taux de glucose dans le sang va redescendre. Par ailleurs, l’insuline retrouve son fonctionnement normal une fois les hormones du stress éliminées.
En cas de maladies infectieuses avec fièvre et un malaise généralisé, le corps sécrète plus d’hormones du stress que d’habitude. Les hormones telles que le cortisol, l’adrénaline, la noradrénaline, l’hormone de croissance et le glucagon entraînent une forte hausse du niveau de glucose. Cette augmentation provoque à son tour un besoin accru en insuline. Si votre température corporelle dépasse les 38°C, le besoin en insuline augmente souvent de 25%; si la fièvre dépasse les 39°C, ce besoin peut même augmenter de plus de 50% par rapport à la quantité d’insuline nécessaire à l’état sain2. Cependant, les personnes souffrant de forte fièvre ont souvent moins d’appétit et ont donc besoin d’une dose réduite d’insuline prandiale (au repas).
Les infections fébriles ne sont pas les seules à augmenter les besoins en insuline. Les infections soi-disant silencieuses telles que les gingivites (inflammations des gencives) peuvent avoir ce même effet. Si vous saignez régulièrement des gencives, nous vous invitons à consulter un dentiste pour exclure une parodontite (une maladie des gencives). Traiter cette affection permet souvent d’améliorer les valeurs de glucose4.
💡 Votre dispositif CGM s’avère très utile en cas de maladie, car il vous permet de surveiller de près toute évolution de vos valeurs de glucose. Ainsi, vous serez en mesure de tolérer des niveaux de glucose très élevés pouvant dépasser les 8,9 mmol/L les jours où vous êtes très malade2. Cependant, vous devriez vérifier votre glycémie régulièrement et la corriger au besoin à l’aide d’insuline à action rapide. Si la dose administrée n’est pas suffisante, votre corps risque de produire trop de cétones et cela augmente la probabilité d’acidocétose diabétique (ACD), un dérèglement métabolique très grave. De ce fait, il est conseillé de mesurer le taux de cétones toutes les 4 à 6 heures afin de garder un œil constant sur le risque d’ACD.3 Pour plus d’informations à ce sujet, nous vous invitons à consulter l’article «Qu’est-ce que l’acidocétose diabétique (ACD)? Et qu’est-ce que le syndrome hyperglycémique hyperosmolaire (SHH)?».
Le cycle menstruel peut affecter les taux de glucose chez certaines femmes, et ce mensuellement. Les hormones œstrogène et progestérone, dont les taux augmentent au cours des jours précédant les règles, entraînent une hausse de la résistance du corps à l’insuline. Cette résistance peut engendrer une augmentation des valeurs de glucose, et donc du besoin en insuline. Ce besoin redescend toutefois à la normale au cours des premiers jours des règles, lorsque les taux d’hormones diminuent.
💡Si vous soupçonnez un lien entre votre cycle menstruel et une hausse de votre glycémie, vérifiez vos valeurs de glucose plus attentivement 1 à 3 jours avant les règles et administrez-vous de l’insuline de correction en cas de valeurs élevées. Les premiers jours des règles, lorsque le besoin en insuline diminue légèrement, il peut être utile de réduire quelque peu la dose d’insuline au repas.
Si vous constatez des valeurs de glucose régulièrement élevées après le même repas, il se peut que le ratio glucides/insuline soit trop faible. Si vous prenez vos repas à la même heure chaque jour, cette cumulation de valeurs constamment trop hautes après le même repas sera visible dans votre profil glycémique ambulatoire (AGP). Pour en savoir plus à ce sujet, nous vous invitons à consulter l’article «Compréhension du rapport AGP».
💡Une dose optimale d’insuline avant le repas devrait vous permettre de corriger l’augmentation des valeurs de glucose (physiologique après un apport en nourriture) grâce à son action en temps utile.
Votre graphique CGM vous aide à comprendre si les affirmations suivantes s’appliquent régulièrement à votre situation:
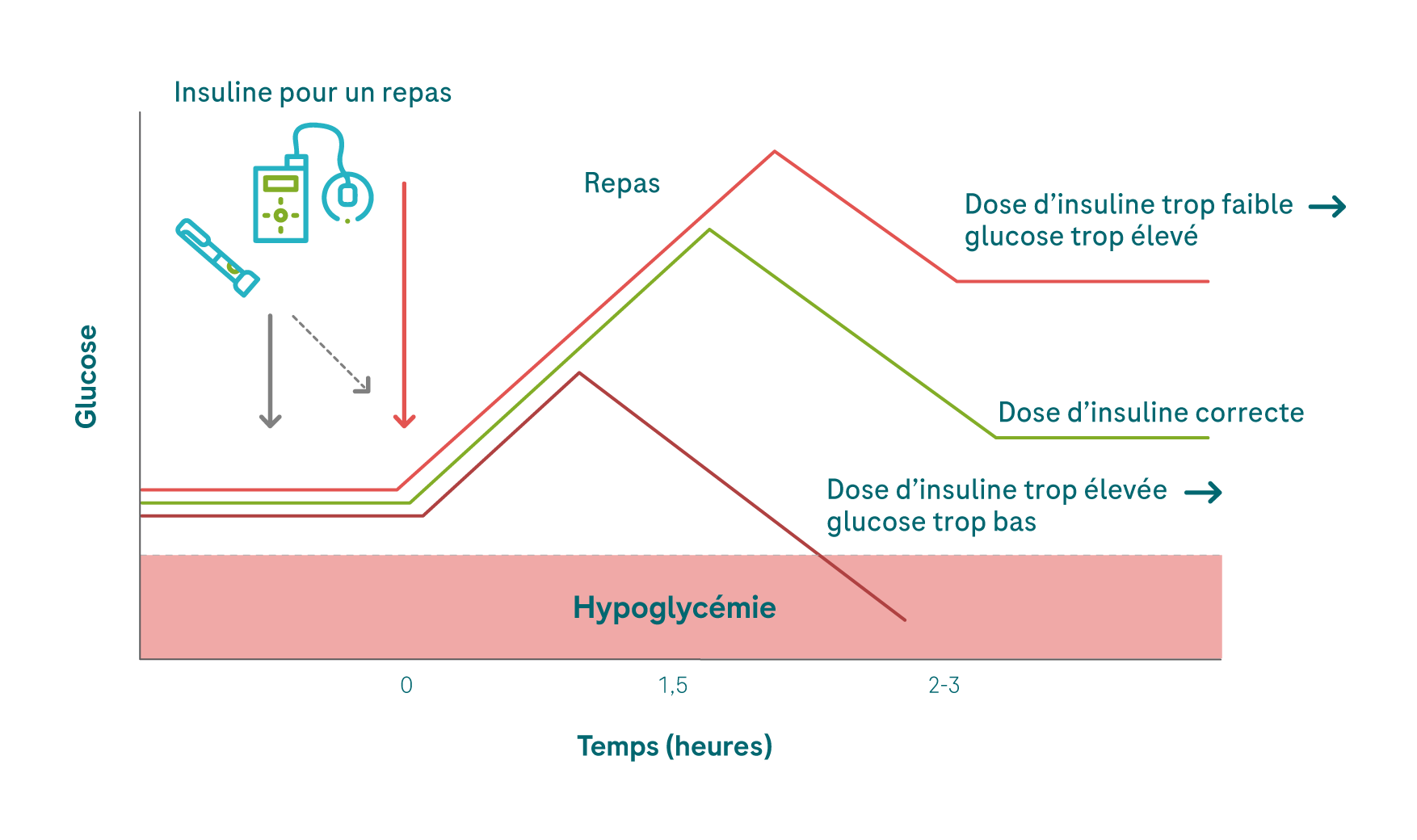
Il est difficile d’estimer la quantité de glucides contenus dans un repas. Même avec beaucoup d’entraînement et d’expérience, vous risquez de vous tromper à chaque fois que vous mangez un nouveau plat ou que vous consommez de la nourriture dont vous ignorez les ingrédients. Les conséquences d’une mauvaise estimation sont évidentes. Si vous estimez une quantité de glucides trop faible, possiblement par crainte de tomber en hypoglycémie, vous vous injectez trop peu d’insuline. Au final, votre valeur de glucose augmentera trop fortement après le repas. Un dispositif CGM vous permet de surveiller aisément l’évolution de vos valeurs après chaque repas et de remarquer immédiatement une éventuelle mauvaise estimation de la quantité de glucides dans votre repas.
💡 Il est toujours utile de se pencher, de temps à autre, sur la quantité de glucides ingérés. Si vous prenez vos repas à la maison, pensez à peser occasionnellement vos portions et à vérifier la quantité de glucides dans les tableaux et les applications destinés à cette fin, ou alors en ligne. Dans le cas des produits transformés, vérifiez la quantité de glucides dans les informations nutritionnelles figurant généralement sur l’emballage.
Une autre cause très fréquente de valeurs élevées après un repas est un oubli d’injection avant d’ingérer de la nourriture. Est-ce que cela vous arrive de temps à autre? Si oui, sachez que vous n’êtes pas le seul à en faire l’expérience, car il s’agit d’un phénomène plus courant que l’on ne croit. Si, après un repas, vous réalisez que vous avez oublié votre injection, ou si vous avez l’habitude de vous injecter votre dose d’insuline après les repas, vos valeurs de glucose seront inévitablement élevées car l’intervalle de temps est trop important entre le moment de l’ingestion de glucides et le moment où l’insuline commence à agir.
💡Gardez votre stylo à insuline à portée de main ou paramétrez une alarme sur votre téléphone pour vous rappeler d’effectuer l’injection avant de prendre votre repas.
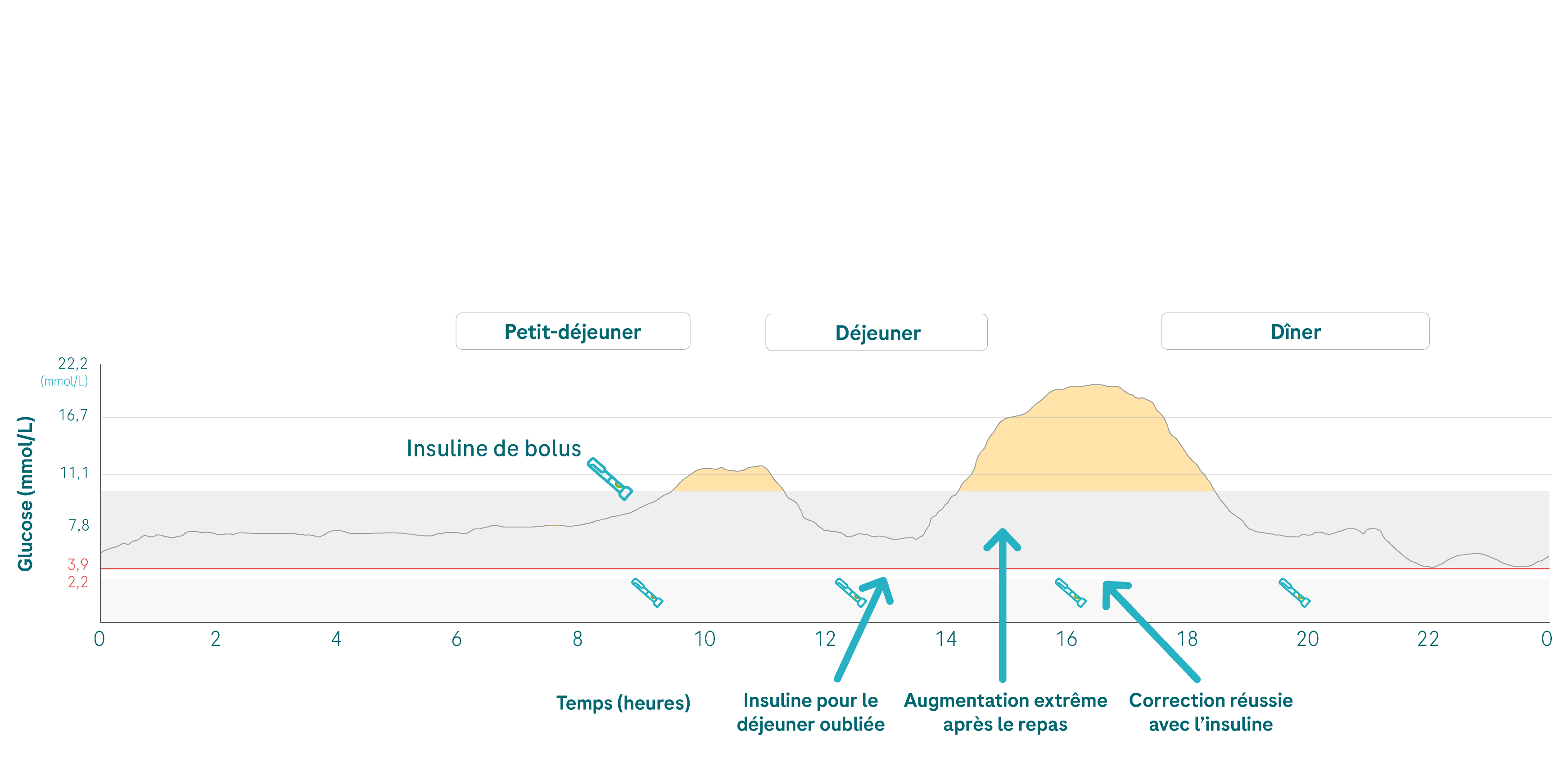
L’intervalle injection-repas est le laps de temps qui sépare le moment de l’injection de la dose d’insuline «repas» et le moment où vous commencez à manger. Dans le passé, seule l’insuline standard était disponible – l’intervalle injection-repas devait donc être scrupuleusement respecté. Pour ce qui est des analogues d’insuline à action rapide couramment utilisés de nos jours, on a longtemps cru que le respect de cet intervalle n’était plus nécessaire. Cependant, si vous regardez l’évolution de vos valeurs CGM de plus près, vous allez constater qu’elles peuvent augmenter drastiquement après un repas en dépit de l'utilisation d’un analogue d’insuline à action rapide.
Votre solution CGM vous permet de déterminer à quelle vitesse et de combien vos valeurs de glucose augmentent. Cela dépend bien entendu également du type de nourriture que vous consommez. Si vous mangez du sucre ou des glucides à absorption rapide sans les associer à des lipides ou protéines, une hausse rapide de vos valeurs de glucose est à attendre.
💡La nécessité ou non de respecter un intervalle injection-repas et la durée de cet intervalle dépendent des facteurs suivants:
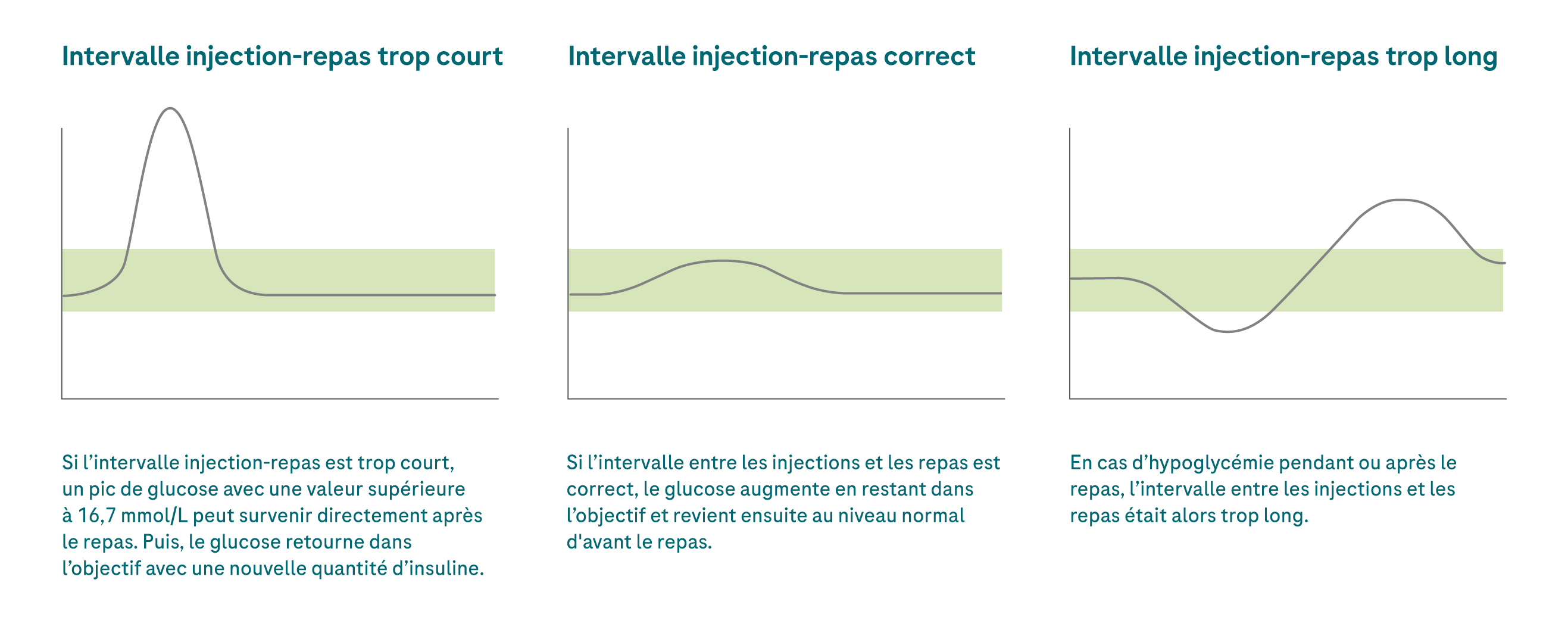
Représentation graphique des différents intervalles injection-repas en supposant que la quantité d’insuline soit correcte et que l’insuline bolus injectée précédemment ne soit plus active.
Consommer un petit en-cas entre les repas ou grignoter une friandise le soir sur son canapé – difficile de résister à ces tentations! Cependant, on oublie souvent de compenser les glucides contenus dans ces aliments par une dose d’insuline correspondante. Il arrive fréquemment d’oublier carrément l’injection, de s’injecter l’insuline avec un certain retard ou alors de corriger l’ingestion de glucides par la suite avec de l’insuline bolus.
💡 L’exercice physique vous permet effectivement de compenser le grignotage sans recourir à l’insuline. Cependant, pendant les périodes d’inactivité comme lorsque vous êtes assis devant l’ordinateur ou la télé, il est nécessaire d’augmenter votre dose d’insuline prandiale (au repas) même pour les petites collations, notamment si votre corps n’est plus en mesure de produire sa propre insuline.
Un dispositif CGM vous permet de déceler ces augmentations plus facilement. Si vous souhaitez perdre du poids, nous vous recommandons d’espacer vos repas et de renoncer complètement aux en-cas – notamment à ceux riches en glucides.
Beaucoup de personnes diabétiques préfèrent s’injecter l’insuline au même site d’injection et n’aiment pas trop changer leurs habitudes. Une sollicitation répétée des mêmes zones de la peau et, par ailleurs, une réutilisation de l’aiguille peuvent altérer le tissu. Cela s’applique également à l’utilisation d’une pompe à insuline, car souvent les patients insèrent le dispositif de perfusion au même site d’injection. De telles habitudes se traduisent souvent en un durcissement palpable du tissu et, dans certains cas, en un épaississement visible appelé lipohypertrophie. Si vous injectez de l’insuline dans une zone de la peu ayant développé une lipohypertrophie, la concentration d’insuline relevée dans le sang peut être réduite d’un tiers par rapport à la concentration en insuline observée après injection dans un tissu sain. Les valeurs de glucose mesurées après un repas seront alors beaucoup plus élevées5
💡Palpez les sites d’injection pour vous assurer de l’absence de gonflements caoutchouteux et d’indurations non visibles à l'œil nu. Évitez ces sites d’injection jusqu’à ce que le tissu soit rétabli – cela peut prendre des mois, voire des années. Lorsque vous changez de site d’injection, une réduction de votre dose d’insuline peut être nécessaire. À ce propos, nous vous invitons à vous consulter avec votre équipe médicale.
Les meilleures stratégies pour éviter une aggravation de la lipohypertrophie sont les suivantes:

Injection dans une zone de lipohypertrophie au niveau de l’abdomen.
[1] Thomas, Andreas et al. (2019). CGM interpretieren: Grundlagen, Technologie, Charakteristik und Konsequenzen des kontinuierlichen Glukosemonitorings (CGM) (2. Aufl.). Mainz
[2] Danne, Thomas et al. (2015). Diabetes bei Kindern und Jugendlichen (7. Aufl.). Heidelberg
[3] American Diabetes Association. Diabetes & DKA (Ketoacidosis). Retrieved November 8, 2022, from https://diabetes.org/diabetes/dka-ketoacidosis-ketones
[4] Baeza M, Morales A, Cisterna C, Cavalla F, Jara G, Isamitt Y, Pino P, Gamonal J. Effect of periodontal treatment in patients with periodontitis and diabetes: systematic review and meta-analysis. J Appl Oral Sci. 2020 Jan 10;28:e20190248. doi: 10.1590/1678-7757-2019-0248. PMID: 31939522; PMCID: PMC6919200.
[5]American Diabetes Association, 6. Glycemic Targets: Standards of Care in Diabetes—2023. Diabetes Care 1 January 2023; 46 (Supplement_1): S97–S110. https://doi.org/10.2337/dc23-S006
[6] Famulla S, Hövelmann U, Fischer A, Coester HV, Hermanski L, Kaltheuner M, Kaltheuner L, Heinemann L, Heise T, Hirsch L. Insulin Injection Into Lipohypertrophic Tissue: Blunted and More Variable Insulin Absorption and Action and Impaired Postprandial Glucose Control. Diabetes Care. 2016 Sep;39(9):1486-92. doi: 10.2337/dc16-0610. Epub 2016 Jul 13. PMID: 27411698.
Vous souhaitez être toujours à jour ? Inscrivez-vous gratuitement dès maintenant !